韓国の研究チームがナノ単位の細胞膜間相互作用を初めて解明した。これを利用すると高感度バイオセンサーの開発が可能になる。
韓国科学技術院(KAIST)は5日、バイオ及び脳工学科のチェ・ミョンチョル教授のチームが、KAIST傘下機関である高等科学院のヒョン・チャンボン教授チーム、浦項加速器研究所のイ・ヒョンフィ博士と共同で、細胞膜間相互作用を媒介する「リピッドラフト(Lipid Raft)」の整列原因と調節メカニズムを初めて解明したと発表しました。
リピッドラフトの原理がわかれば、細胞融合、ウイルス侵入、細胞間シグナル伝達などの多様な細胞膜間相互作用を調節することができる。
リピッドラフトは細胞膜に存在するナノメートルサイズの領域で、周囲に比べてコレステロール濃度が高く、脂質分子がより密集した状況で構成されている。
チェ・ミョンチョル教授は「細胞膜を海に、膜タンパク質を人に例えてみる。すると、大海原で遠く離れて泳いでいる人たち同士は意思疎通が難しい。だが、彼らを一つのいかだに乗せれば、互いに簡単に会話できるのと同じ原理だと理解できる」と説明する。
チェ教授はまた「リピッドラフト上のタンパク質がウイルス初期接触および侵入地点」と指摘している。
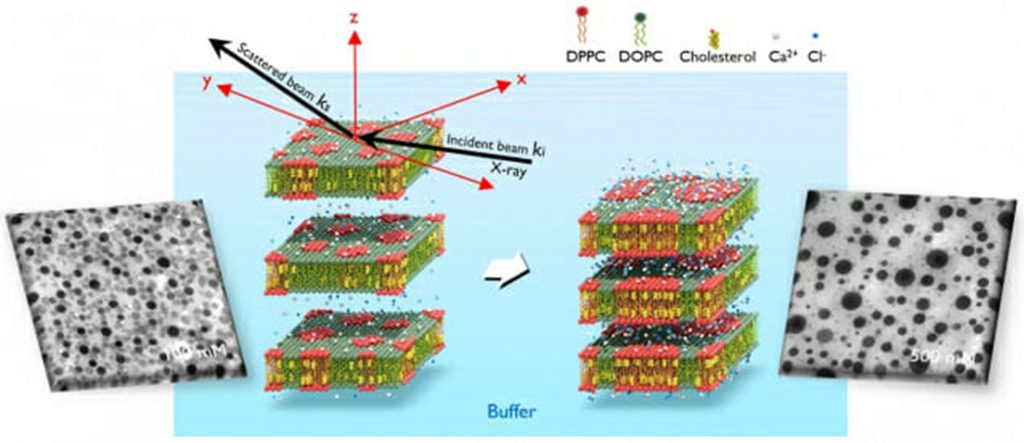
研究チームは二つの細胞膜の相互作用を模写するため、シリコンウェーハ上に相分離脂質多重膜の形でリピッドラフトを再現した。膜間距離調節には静電力と浸透圧を利用した。また、膜間距離の測定には蛍光顕微鏡とX線反射率を活用した。
チームは研究を通じて、二つの細胞膜間の距離がリピッドラフトの整列と大きさを調節する核心スイッチであることを解明した。
チェ教授は「リピッドラフトがどのような原理で相互作用を媒介するのかを初めて解明したものであり、人体の70%を占める水分子の水素結合がリピッドラフトの整列を媒介する核心要素であることも明らかにした」としている。
チームは「細胞膜間の距離というスイッチ調節を通じて、より多様な機能を持つバイオセンサーを開発できる工学的基盤も提供できる」と見通している。
(c)KOREA WAVE